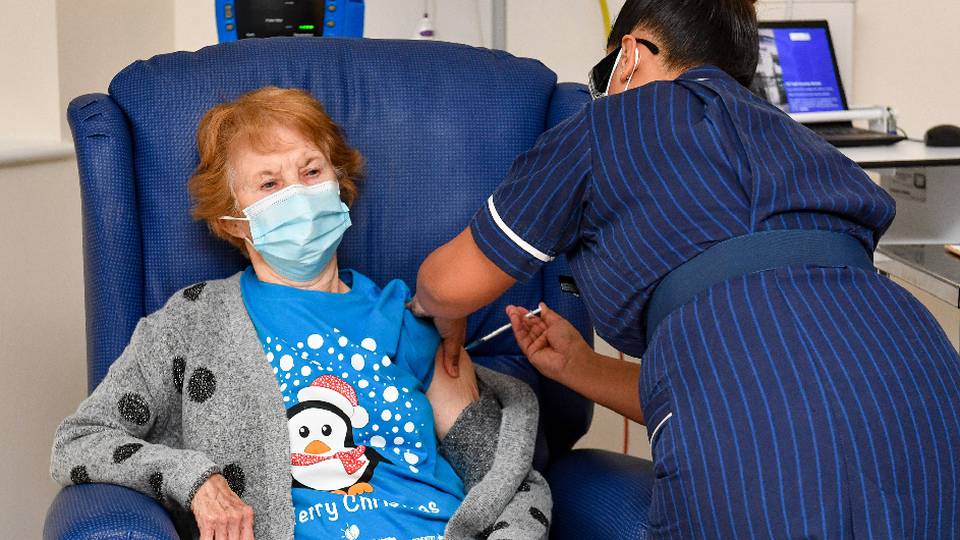
Una británica de 90 años se convirtió en la primera paciente del mundo en recibir la vacuna contra la covid-19 desarrollada por Pfizer y BioNTech.
Responsables del servicio de sanidad pública británico advirtieron este miércoles de que las personas con un historial de reacciones alérgicas significativas no deberían recibir de momento la vacuna contra la covid-19 desarrollada por Pfizer/BioNTech.
La advertencia se produjo después de que dos trabajadores del Servicio Nacional de Salud (NHS) británico, que estuvieron entre los primeros en recibir la vacuna el martes, sufrieran reacciones alérgicas y necesitaran tratamiento.
El director médico del NHS en Inglaterra, Stephen Powis, explicó que ambas personas, que tenían un historial de alergias, se estaban recuperando correctamente.
La Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA), organismo independiente británico que la semana pasada se convirtió en el primero del mundo en autorizar esta vacuna, ha aconsejado ahora que “las personas con un historial significativo de reacciones alérgicas no la reciban” como precaución, añadió.
Las reacciones alérgicas “significativas” incluyen medicamentos, alimentos o vacunas, según la MHRA.
El martes, miles de habitantes del Reino Unido se convirtieron en los primeros del mundo occidental en recibir una vacuna contra la covid-19, cuando el NHS comenzó la mayor campaña de vacunación desde su creación en 1948.
La vacuna de Pfizer/BioNTech se administra en dos dosis, con 21 días de diferencia. Las personas mayores de 80 años, sus cuidadores y el personal sanitario son los primeros designados para ser vacunados.
El país ha recibido unas 800.000 dosis de la vacuna en el primer lote de un pedido total de 40 millones que debe ir llegando progresivamente en los próximos meses.
El director ejecutivo de Pfizer, Albert Bourla, dijo el martes que entendía la inquietud internacional por la velocidad con la que las compañías farmacéuticas han producido vacunas contra el coronavirus. Pero insistió en que se respetaron todos los protocolos de seguridad.
Pfizer afirmó que el MHRA les había informado de las reacciones alérgicas, pero que durante los ensayos clínicos de fase 3 en más de 40.000 personas, la vacuna fue “generalmente bien tolerada, sin que se hayan registrado problemas de seguridad graves”.
Las dudas que tiene Pfizer tras anunciar la vacuna contra el coronavirus
En días pasados un estudio de casi 44.000 personas mostró que la vacuna de Pfizer previno el 95 por ciento de los casos de coronavirus sintomáticos y, de acuerdo con la compañía, no hubo problemas de seguridad importantes.
De hecho, Albert Bourla, director ejecutivo de Pfizer, dijo en su momento que los resultados del estudio marcaban “un paso importante en este histórico viaje de ocho meses para presentar una vacuna capaz de ayudar a poner fin a esta devastadora pandemia”. De acuerdo con Pfizer, la eficacia del casi 100 por ciento se refleja a partir de 28 días después de la primera dosis.

Sin embargo, en entrevista con el presentador de Dateline, Lester Holt, Bourla dijo que la empresa “no estaba segura” si la vacuna contra el coronavirus impedía finalmente la transmisión del virus, por lo que advirtió que era algo que tocaba examinarse.
El presentador le preguntó a Bourla: “Aunque he tenido la protección, ¿todavía puedo transmitirla a otras personas?”, y el presidente de Pfizer le respondió: “Creo que esto es algo que debe examinarse. No estamos seguros de eso en este momento con lo que sabemos”.